

Оставить заявку
Оставить заявку
Мы используем cookie и сервисы веб-аналитики для работы сайта, анализа посещаемости и улучшения сервиса. Продолжая пользоваться сайтом, вы соглашаетесь с использованием cookie. Подробнее в Политике обработки персональных данных.

ОСТАВИТЬ ЗАЯВКУ
Заполняя данную форму, вы соглашаетесь с Правилами обработки персональных данных
Холодная атмосферная плазма: биохакинг кожи на молекулярном уровне

16 Апреля 2026

Новые технологии красоты
01
Введение
Холодная атмосферная плазма (ХАП) представляет собой физический агент с уникальным профилем биологической активности: одно воздействие одновременно модулирует несколько независимых молекулярных программ в клетках кожи. С этой точки зрения ХАП соответствует логике биохакинга — то есть целенаправленной регуляции биологических систем через контролируемое воздействие на клеточные сигнальные пути. В отличие от фармакологических агентов с направленным механизмом действия и большинства энергетических эстетических технологий, воздействующих на одну тканевую мишень, ХАП инициирует параллельные сигнальные ответы — через редокс-зависимые каскады, транскрипционные регуляторы и межклеточные медиаторы.
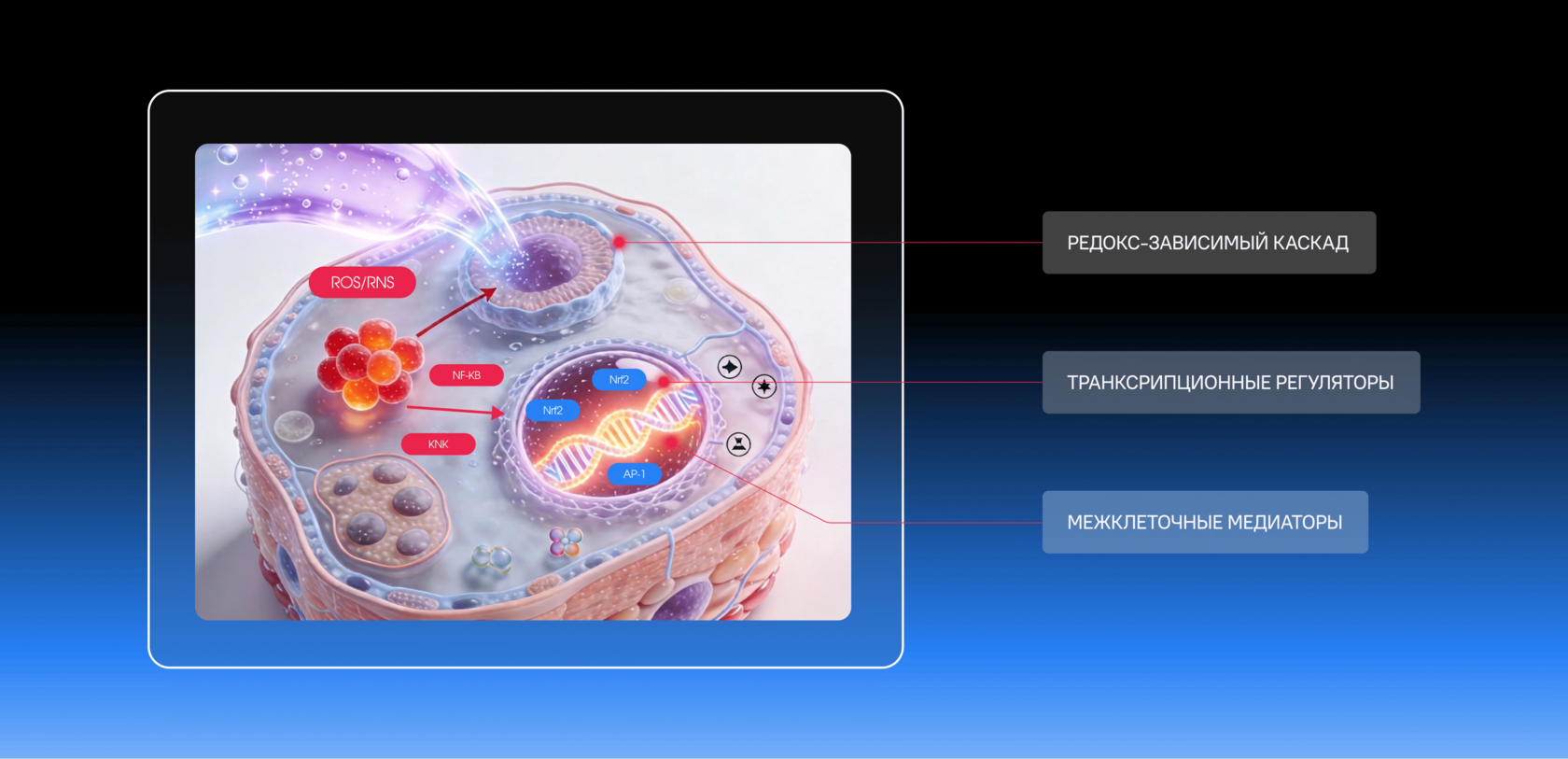
Накопленная к настоящему времени доказательная база охватывает девять задокументированных механизмов: от активации Nrf2-зависимой антиоксидантной защиты и подавления NF-κB-опосредованного воспаления до регуляции меланогенеза, восстановления барьерной функции эпидермиса, модуляции NO-зависимого сосудистого ответа и широкоспектральной противомикробной активности без риска формирования резистентности. Каждый механизм подтверждён в независимых экспериментальных или клинических исследованиях и опирается на идентифицированные молекулярные мишени.
02
Механизм 1. Антиоксидантная перепрошивка клеток
ХАП через умеренный оксидативный и нитрозативный стресс способен активировать Nrf2 — ключевой транскрипционный регулятор антиоксидантной защиты клетки. В ответ усиливается экспрессия ферментов антиоксидантной системы, включая супероксиддисмутазу (SOD), каталазу и глутатионпероксидазу. Также в ряде моделей показано вовлечение глутатионового метаболизма и повышение активности систем, связанных с его синтезом и регенерацией. Эти изменения рассматриваются не только как краткосрочная нейтрализация реактивных форм, но и как элемент адаптивного клеточного ответа на контролируемый стресс [1−3].
Холодная плазма генерирует активные формы кислорода (в том числе перекисные соединения и супероксид) и азота (NO и его производные), которые могут сохраняться в тканях в виде более стабильных метаболитов (NO, NO₂). Эти соединения участвуют в формировании редокс-сигналов и могут запускать каскады клеточной адаптации, включая активацию Nrf2-зависимых путей [2, 4]. Важно, что характер ответа зависит от дозы воздействия: при умеренных параметрах преобладает адаптивный и защитный эффект, тогда как при высоких — возможно истощение антиоксидантных систем.
Таким образом, плазменное воздействие можно рассматривать как способ модуляции собственной антиоксидантной системы кожи за счёт запуска эндогенных защитных механизмов.
Холодная плазма генерирует активные формы кислорода (в том числе перекисные соединения и супероксид) и азота (NO и его производные), которые могут сохраняться в тканях в виде более стабильных метаболитов (NO, NO₂). Эти соединения участвуют в формировании редокс-сигналов и могут запускать каскады клеточной адаптации, включая активацию Nrf2-зависимых путей [2, 4]. Важно, что характер ответа зависит от дозы воздействия: при умеренных параметрах преобладает адаптивный и защитный эффект, тогда как при высоких — возможно истощение антиоксидантных систем.
Таким образом, плазменное воздействие можно рассматривать как способ модуляции собственной антиоксидантной системы кожи за счёт запуска эндогенных защитных механизмов.
Источники
[1] Schmidt A, Dietrich S, Steuer A et al. Non-thermal Plasma Activates Human Keratinocytes by Stimulation of Antioxidant and Phase II Pathways. J Biol Chem. 2015;290(11):6731−6750. PMID: 25 589 789.
[2] Schmidt A, von Woedtke T, Stenzel J et al. Nrf2 signaling and inflammation are key events in physical plasma-spurred wound healing. Theranostics. 2019;9(4):1066−1084. DOI: 10.7150/thno.29 754.
[3] Bekeschus S, Schmidt A, Kramer A, Metelmann HR. Redox regulation of wound healing: role of cold physical plasma and Nrf2 signaling. Antioxidants. 2018;7(10):146. DOI: 10.3390/antiox7100146.
[4] Graves DB. Reactive species from cold atmospheric plasma: implications for cancer therapy. Plasma Process Polym. 2014;11(12):1120−1127. DOI: 10.1002/ppap.201 400 068.
[2] Schmidt A, von Woedtke T, Stenzel J et al. Nrf2 signaling and inflammation are key events in physical plasma-spurred wound healing. Theranostics. 2019;9(4):1066−1084. DOI: 10.7150/thno.29 754.
[3] Bekeschus S, Schmidt A, Kramer A, Metelmann HR. Redox regulation of wound healing: role of cold physical plasma and Nrf2 signaling. Antioxidants. 2018;7(10):146. DOI: 10.3390/antiox7100146.
[4] Graves DB. Reactive species from cold atmospheric plasma: implications for cancer therapy. Plasma Process Polym. 2014;11(12):1120−1127. DOI: 10.1002/ppap.201 400 068.
03
Механизм 2. Подавление inflammaging - хронического воспаления
Холодная атмосферная плазма способна влиять на воспалительные процессы через редокс-зависимые механизмы регуляции. В частности, активация Nrf2 ассоциирована с подавлением активности NF-κB — одного из основных транскрипционных факторов, контролирующих экспрессию провоспалительных цитокинов [1,2].
В экспериментальных моделях показано, что плазменное воздействие приводит к снижению экспрессии таких медиаторов воспаления, как IL-6, IL-8 и TNF-α, а также к модуляции клеточного ответа на воспалительный стимул [1−3]. Это позволяет рассматривать эффект не только как симптоматическое уменьшение воспаления, но и как изменение регуляции воспалительных путей на уровне клеточного сигнального ответа.
Таким образом, плазменное воздействие может участвовать в перераспределении баланса между провоспалительными и защитными сигналами, что потенциально важно в контексте возраст-ассоциированного воспаления кожи.
В экспериментальных моделях показано, что плазменное воздействие приводит к снижению экспрессии таких медиаторов воспаления, как IL-6, IL-8 и TNF-α, а также к модуляции клеточного ответа на воспалительный стимул [1−3]. Это позволяет рассматривать эффект не только как симптоматическое уменьшение воспаления, но и как изменение регуляции воспалительных путей на уровне клеточного сигнального ответа.
Таким образом, плазменное воздействие может участвовать в перераспределении баланса между провоспалительными и защитными сигналами, что потенциально важно в контексте возраст-ассоциированного воспаления кожи.
Источники
[1] Schmidt A, von Woedtke T, Stenzel J et al. Nrf2 signaling and inflammation are key events in physical plasma-spurred wound healing. Theranostics. 2019;9(4):1066–1084. DOI: 10.7150/thno.29754.
[2] Bekeschus S, Schmidt A, Kramer A, Metelmann HR. Redox regulation of wound healing: role of cold physical plasma and Nrf2 signaling. Antioxidants. 2018;7(10):146. DOI: 10.3390/antiox7100146.
[3] Schmidt A, Dietrich S, Steuer A et al. Non-thermal Plasma Activates Human Keratinocytes by Stimulation of Antioxidant and Phase II Pathways. J Biol Chem. 2015;290(11):6731–6750. PMID: 25589789.
[2] Bekeschus S, Schmidt A, Kramer A, Metelmann HR. Redox regulation of wound healing: role of cold physical plasma and Nrf2 signaling. Antioxidants. 2018;7(10):146. DOI: 10.3390/antiox7100146.
[3] Schmidt A, Dietrich S, Steuer A et al. Non-thermal Plasma Activates Human Keratinocytes by Stimulation of Antioxidant and Phase II Pathways. J Biol Chem. 2015;290(11):6731–6750. PMID: 25589789.
04
Механизм 3. Стимуляция фибробластов, синтез матрикса и морфологическое омоложение дермы
Фибробласты являются ключевыми клетками, поддерживающими структурную организацию дермы и обеспечивающими синтез компонентов внеклеточного матрикса. В экспериментальных моделях показано, что воздействие аргоновой ХАП сопровождается увеличением экспрессии генов, связанных с матриксом, включая коллаген I типа, фибронектин и сосудистый эндотелиальный фактор роста (VEGF), без признаков выраженного клеточного повреждения. Эти молекулы играют важную роль в поддержании структуры дермы, клеточной адгезии и регуляции ангиогенеза [1]: коллаген I составляет более 90% органической материи кожи, фибронектин обеспечивает связь клеток с матриксом, VEGF стимулирует ангиогенез для питания восстанавливающихся тканей.
Дополнительно в гистологическом исследовании парных биоптатов гипертрофического рубца после воздействия аргоновой плазмы продемонстрировано увеличение доли коллагена III типа, подтверждённое иммуногистохимически [2]. Коллаген III ассоциирован с ранними этапами ремоделирования внеклеточного матрикса, и его увеличение может отражать активацию процессов перестройки ткани.
Морфологически эти изменения сопровождались переходом от дезорганизованного расположения коллагеновых волокон к более упорядоченной структуре с параллельной ориентацией пучков, а также снижением выраженности воспалительного инфильтрата [2]. Эти данные интерпретируются как признаки ремоделирования дермального матрикса в зоне воздействия.
В отношении азотной плазмы показано, что при низкоэнергетических режимах она может способствовать активации клеточной пролиферации и ускорению репаративных процессов, что связывают с действием реактивных форм азота и модуляцией клеточных сигнальных путей [3].
Таким образом, различные типы плазменного воздействия могут оказывать комплементарное влияние на дерму: аргоновая плазма — преимущественно на уровне регуляции синтеза и организации матрикса, а азотная — на уровне клеточной активности и репарации тканей. Комбинация аргон+азот обеспечивает и стимуляцию синтеза, и качество синтезируемого матрикса.
Дополнительно в гистологическом исследовании парных биоптатов гипертрофического рубца после воздействия аргоновой плазмы продемонстрировано увеличение доли коллагена III типа, подтверждённое иммуногистохимически [2]. Коллаген III ассоциирован с ранними этапами ремоделирования внеклеточного матрикса, и его увеличение может отражать активацию процессов перестройки ткани.
Морфологически эти изменения сопровождались переходом от дезорганизованного расположения коллагеновых волокон к более упорядоченной структуре с параллельной ориентацией пучков, а также снижением выраженности воспалительного инфильтрата [2]. Эти данные интерпретируются как признаки ремоделирования дермального матрикса в зоне воздействия.
В отношении азотной плазмы показано, что при низкоэнергетических режимах она может способствовать активации клеточной пролиферации и ускорению репаративных процессов, что связывают с действием реактивных форм азота и модуляцией клеточных сигнальных путей [3].
Таким образом, различные типы плазменного воздействия могут оказывать комплементарное влияние на дерму: аргоновая плазма — преимущественно на уровне регуляции синтеза и организации матрикса, а азотная — на уровне клеточной активности и репарации тканей. Комбинация аргон+азот обеспечивает и стимуляцию синтеза, и качество синтезируемого матрикса.
Источники
[1] Kim HY, Agrahari G, Lee MJ et al. Low-Temperature Argon Plasma Regulates Skin Moisturizing and Melanogenesis-Regulating Markers through Yes-Associated Protein. Int J Mol Sci. 2021;22(4):1895. PMID: 33672928.
[2] Гистологическое исследование воздействия аргоновой плазмы на гипертрофический рубец: https://pladuo.ru/scarhistology
[3] Обзор механизмов действия аргоновой и азотной плазмы: https://pladuo.ru/argonandnitrogenplasma
[2] Гистологическое исследование воздействия аргоновой плазмы на гипертрофический рубец: https://pladuo.ru/scarhistology
[3] Обзор механизмов действия аргоновой и азотной плазмы: https://pladuo.ru/argonandnitrogenplasma
05
Механизм 4. Блокировка деградации внеклеточного матрикса
Матриксные металлопротеиназы (MMP) представляют собой группу ферментов, участвующих в деградации компонентов внеклеточного матрикса, включая коллаген и эластин. В ряде экспериментальных работ показано, что воздействие холодной атмосферной плазмы (ХАП) может сопровождаться снижением экспрессии MMP, что связывают с модуляцией сигнальных путей, регулирующих воспалительный ответ, в частности с уменьшением активности NF-κB [1,2].
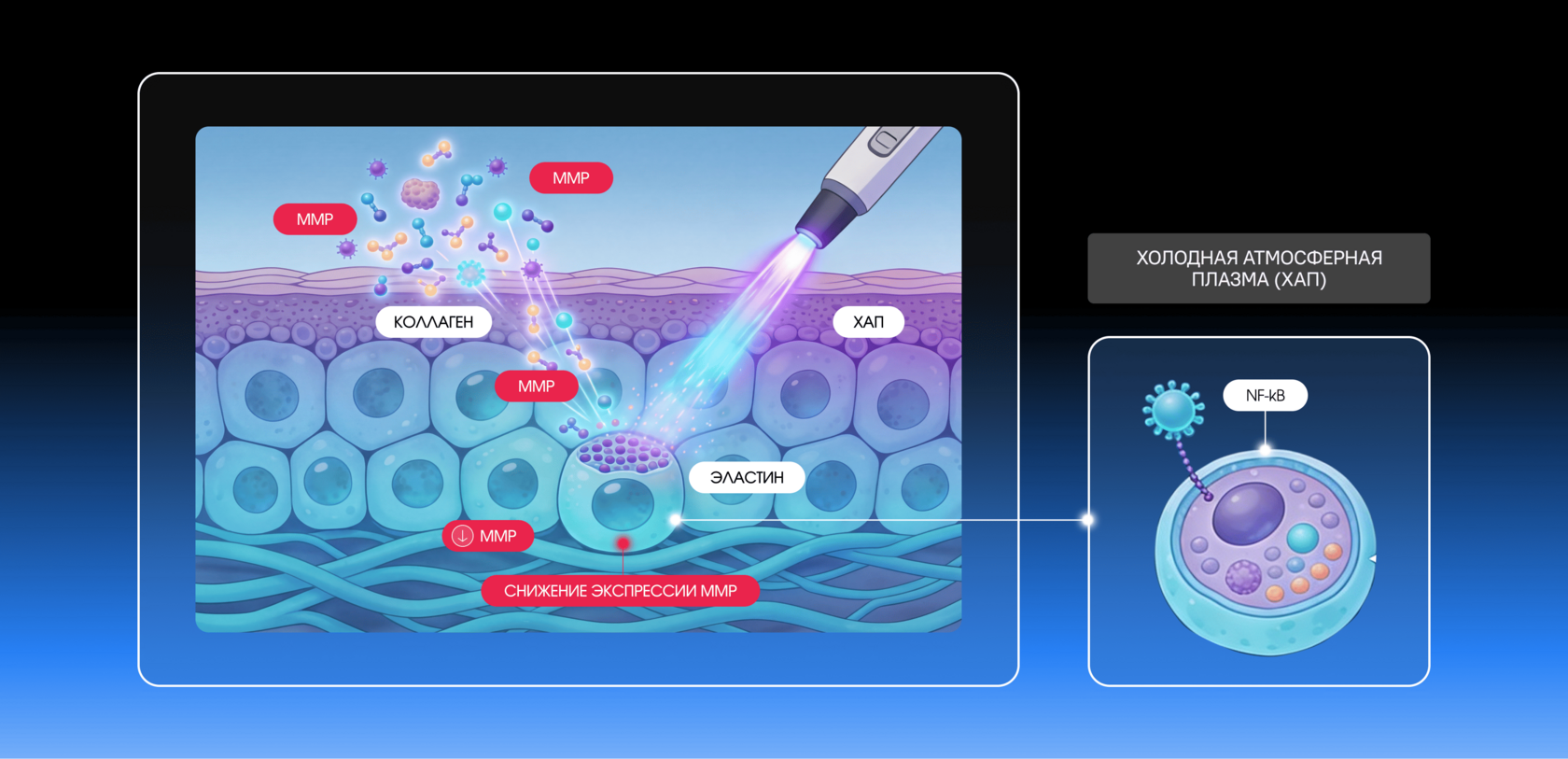
Дополнительно продемонстрировано, что низкотемпературная аргоновая плазма способна снижать экспрессию отдельных представителей семейства MMP, включая MMP-3, что ассоциировано с изменениями в активности сигнального пути YAP/Hippo [3]. Снижение экспрессии MMP-3 рассматривается как потенциальный механизм ограничения деградации матрикса.
Отдельное внимание в современных исследованиях уделяется влиянию плазмы на клеточное старение и связанный с ним секреторный фенотип (SASP). Сенесцентные клетки характеризуются повышенной продукцией провоспалительных цитокинов и протеаз, включая MMP, что способствует распространению дегенеративных изменений в тканях. Имеются данные, что ХАП может снижать выраженность SASP и тем самым ограничивать паракринное влияние сенесцентных клеток на окружающие ткани [2,4].
Таким образом, воздействие холодной плазмы может рассматриваться как фактор, способствующий снижению матриксной деградации и модуляции возраст-ассоциированных изменений в дерме за счёт влияния на экспрессию MMP и связанные с ними сигнальные каскады.
Отдельное внимание в современных исследованиях уделяется влиянию плазмы на клеточное старение и связанный с ним секреторный фенотип (SASP). Сенесцентные клетки характеризуются повышенной продукцией провоспалительных цитокинов и протеаз, включая MMP, что способствует распространению дегенеративных изменений в тканях. Имеются данные, что ХАП может снижать выраженность SASP и тем самым ограничивать паракринное влияние сенесцентных клеток на окружающие ткани [2,4].
Таким образом, воздействие холодной плазмы может рассматриваться как фактор, способствующий снижению матриксной деградации и модуляции возраст-ассоциированных изменений в дерме за счёт влияния на экспрессию MMP и связанные с ними сигнальные каскады.
Источники
[1] Schmidt A, von Woedtke T, Stenzel J et al. Nrf2 signaling and inflammation are key events in physical plasma-spurred wound healing. Theranostics. 2019;9(4):1066–1084. DOI: 10.7150/thno.29754.
[2] Bekeschus S, Schmidt A, Kramer A, Metelmann HR. Redox regulation of wound healing: role of cold physical plasma and Nrf2 signaling. Antioxidants. 2018;7(10):146. DOI: 10.3390/antiox7100146.
[3] Kim HY, Agrahari G, Lee MJ et al. Low-Temperature Argon Plasma Regulates Skin Moisturizing and Melanogenesis-Regulating Markers through Yes-Associated Protein. Int J Mol Sci. 2021;22(4):1895. PMID: 33672928.
[4] Arndt S, Unger P, Wacker E et al. Cold atmospheric plasma (CAP) changes gene expression of key molecules of the wound healing machinery and improves wound healing in vitro and in vivo. PLoS One. 2013;8(11):e79325. DOI: 10.1371/journal.pone.0079325.
[2] Bekeschus S, Schmidt A, Kramer A, Metelmann HR. Redox regulation of wound healing: role of cold physical plasma and Nrf2 signaling. Antioxidants. 2018;7(10):146. DOI: 10.3390/antiox7100146.
[3] Kim HY, Agrahari G, Lee MJ et al. Low-Temperature Argon Plasma Regulates Skin Moisturizing and Melanogenesis-Regulating Markers through Yes-Associated Protein. Int J Mol Sci. 2021;22(4):1895. PMID: 33672928.
[4] Arndt S, Unger P, Wacker E et al. Cold atmospheric plasma (CAP) changes gene expression of key molecules of the wound healing machinery and improves wound healing in vitro and in vivo. PLoS One. 2013;8(11):e79325. DOI: 10.1371/journal.pone.0079325.
06
Механизм 5. Восстановление кожного барьера и увлажнённости через YAP
Кожный барьер — это не просто физическая плёнка. Его состоятельность определяется активной работой эпидермальных клеток: синтезом структурных белков, производством гиалуроновой кислоты и постоянным обновлением межклеточного матрикса. Когда эта работа нарушается, кожа теряет влагу, становится уязвимой к внешним раздражителям и хуже восстанавливается.
В исследовании на кератиноцитах и дермальных фибробластах человека низкотемпературная аргоновая плазма повышала экспрессию ключевых барьерных маркеров: филагрина и инволюкрина — белков, обеспечивающих плотность рогового слоя, — а также трансглутаминазы и гиалуронансинтаз HAS1 и HAS2, ответственных за синтез гиалуроновой кислоты в эпидермисе. Молекулярным посредником этих эффектов выступал YAP — транскрипционный регулятор, контролирующий пролиферацию и дифференцировку клеток кожи: при его блокировании описанные эффекты плазмы ослабевали [1].
Практически важно, что речь идёт не о внешнем восполнении влаги, а о стимуляции собственных молекулярных программ клетки. Аргоновая плазма в данном контексте работает как биологический триггер — активирует эндогенные механизмы, которые кожа использует для самовосстановления.
В исследовании на кератиноцитах и дермальных фибробластах человека низкотемпературная аргоновая плазма повышала экспрессию ключевых барьерных маркеров: филагрина и инволюкрина — белков, обеспечивающих плотность рогового слоя, — а также трансглутаминазы и гиалуронансинтаз HAS1 и HAS2, ответственных за синтез гиалуроновой кислоты в эпидермисе. Молекулярным посредником этих эффектов выступал YAP — транскрипционный регулятор, контролирующий пролиферацию и дифференцировку клеток кожи: при его блокировании описанные эффекты плазмы ослабевали [1].
Практически важно, что речь идёт не о внешнем восполнении влаги, а о стимуляции собственных молекулярных программ клетки. Аргоновая плазма в данном контексте работает как биологический триггер — активирует эндогенные механизмы, которые кожа использует для самовосстановления.
Источники
[1] Kim HY, Agrahari G, Lee MJ et al. Low-Temperature Argon Plasma Regulates Skin Moisturizing and Melanogenesis-Regulating Markers through Yes-Associated Protein. Int J Mol Sci. 2021;22(4):1895. PMID: 33672928.
07
Механизм 6. Многоуровневый контроль пигментации
Синтез меланина — сложный многоступенчатый процесс с несколькими точками регуляции. Ключевые участники хорошо известны: рецептор MC1R, принимающий гормональный сигнал от α-МСГ; транскрипционный фактор MITF, включающий гены пигментных ферментов; тирозиназа — фермент, запускающий синтез меланина из тирозина; и глутатион — внутриклеточный антиоксидант, способный перехватывать промежуточные продукты меланогенеза. Нетепловая холодная атмосферная плазма может взаимодействовать с несколькими из этих звеньев — по-разному в зависимости от типа газа-носителя [1−4].
Путь I. Аргоновая плазма: подавление гормонального сигнала через YAP → MC1R → MITF
Чтобы меланоцит начал производить меланин, он должен сначала получить сигнал. Главным его источником служит гормон α-МСГ, который связывается с рецептором MC1R на поверхности меланоцита и запускает внутриклеточный каскад: PKA → CREB → MITF → тирозиназа. MITF при этом играет роль главного дирижёра — именно он включает гены всех ключевых меланогенных ферментов: тирозиназы, TRP-1 и TRP-2.
В экспериментах на клеточных линиях B16F10 и первичных меланоцитах человека (NHEM) было показано, что низкотемпературная аргоновая плазма (LTAP) снижает экспрессию белка YAP в меланоцитах. YAP — транскрипционный коактиватор сигнального пути Hippo — поддерживает экспрессию MC1R. После воздействия аргоновой плазмы чувствительность меланоцитов к α-МСГ достоверно падала: фосфорилирование PKA и CREB уменьшалось, а вместе с ним снижалась экспрессия MITF, тирозиназы и TRP-1 на уровне и мРНК, и белка. Содержание меланина в клетках при этом достоверно уменьшалось [1]. Примечательно, что в кератиноцитах и дермальных фибробластах тот же LTAP, напротив, повышает YAP — усиливая синтез коллагена и барьерных белков кожи. Эффект строго клеточно-специфичен и в меланоцитах направлен исключительно на подавление пигментации.
В экспериментах на клеточных линиях B16F10 и первичных меланоцитах человека (NHEM) было показано, что низкотемпературная аргоновая плазма (LTAP) снижает экспрессию белка YAP в меланоцитах. YAP — транскрипционный коактиватор сигнального пути Hippo — поддерживает экспрессию MC1R. После воздействия аргоновой плазмы чувствительность меланоцитов к α-МСГ достоверно падала: фосфорилирование PKA и CREB уменьшалось, а вместе с ним снижалась экспрессия MITF, тирозиназы и TRP-1 на уровне и мРНК, и белка. Содержание меланина в клетках при этом достоверно уменьшалось [1]. Примечательно, что в кератиноцитах и дермальных фибробластах тот же LTAP, напротив, повышает YAP — усиливая синтез коллагена и барьерных белков кожи. Эффект строго клеточно-специфичен и в меланоцитах направлен исключительно на подавление пигментации.
Путь II. Нетепловая плазма: активация Nrf2 и вовлечение глутатионового метаболизма → переключение с эумеланина на феомеланин
Любая нетепловая плазма генерирует активные формы кислорода и азота в субтоксических концентрациях. Этого достаточно, чтобы активировать транскрипционный фактор Nrf2 — ключевой клеточный сенсор окислительного стресса, запускающий экспрессию антиоксидантных ферментов. В экспериментах на кератиноцитах человека (HaCaT и NHEK) после плазменного воздействия была показана ядерная транслокация Nrf2, активация путей второй фазы антиоксидантной защиты и изменения, связанные с глутатионовым метаболизмом [2].
Это создаёт биологические предпосылки для влияния на химию меланина. Тиольная группа глутатиона может реагировать с допахиноном — промежуточным продуктом, образуемым тирозиназой, — и перенаправлять реакцию в сторону феомеланина вместо эумеланина. Кроме того, глутатион способен взаимодействовать с активным центром тирозиназы и модифицировать её активность. Важный нюанс состоит в том, что этот эффект зависит от концентрации: поэтому механизм точнее описывать не как универсальное прямое ингибирование тирозиназы, а как сочетание перехвата промежуточных продуктов меланогенеза и модуляции ферментативной активности [3, 4].
Это создаёт биологические предпосылки для влияния на химию меланина. Тиольная группа глутатиона может реагировать с допахиноном — промежуточным продуктом, образуемым тирозиназой, — и перенаправлять реакцию в сторону феомеланина вместо эумеланина. Кроме того, глутатион способен взаимодействовать с активным центром тирозиназы и модифицировать её активность. Важный нюанс состоит в том, что этот эффект зависит от концентрации: поэтому механизм точнее описывать не как универсальное прямое ингибирование тирозиназы, а как сочетание перехвата промежуточных продуктов меланогенеза и модуляции ферментативной активности [3, 4].
Путь III. Азотная плазма: клинически задокументированный антипигментный эффект при рефрактерной мелазме
Азотная плазма генерирует преимущественно активные формы азота (RNS) и оказывает контролируемый термический эффект на эпидермис. В клиническом наблюдении с использованием микроволнового (2,45 ГГц) азотного плазменного генератора PLADUO у трёх пациентов с рефрактерной периорбитальной мелазмой — не ответивших ни на топические осветляющие агенты, ни на Nd: YAG-лазер — было зафиксировано выраженное клиническое улучшение пигментации [5]. Это принципиально важный клинический факт: речь идёт именно о рефрактерных случаях, то есть о пациентах, у которых стандартные подходы к ингибированию тирозиназы исчерпали свой потенциал.
На уровне молекулярных механизмов показано, что плазма-активированные соединения способны изменять активность тирозиназы и снижать уровень меланогенеза в клетках меланомы — это продемонстрировано как в бесклеточных системах, так и в клеточной модели B16F10 [6]. В частности, наблюдалось снижение активности тирозиназы и содержания меланина, а также изменения её структурных характеристик. При этом в данных работах использовались плазма-активированные соединения, а не прямое воздействие азотной плазмы, что указывает на возможный, но не окончательно подтверждённый перенос этих механизмов на клинический эффект.
На уровне молекулярных механизмов показано, что плазма-активированные соединения способны изменять активность тирозиназы и снижать уровень меланогенеза в клетках меланомы — это продемонстрировано как в бесклеточных системах, так и в клеточной модели B16F10 [6]. В частности, наблюдалось снижение активности тирозиназы и содержания меланина, а также изменения её структурных характеристик. При этом в данных работах использовались плазма-активированные соединения, а не прямое воздействие азотной плазмы, что указывает на возможный, но не окончательно подтверждённый перенос этих механизмов на клинический эффект.
08
Вывод: три уровня регуляции, два газа
Совокупность представленных данных позволяет охарактеризовать воздействие аргоновой и азотной плазмы на меланогенез на трёх независимых уровнях.
Аргоновая плазма действует на уровне гормонального рецептора и транскрипционного контроля: подавляет YAP в меланоцитах → снижает MC1R → ослабляет α-МСГ-зависимую активацию PKA/CREB/MITF → уменьшает экспрессию тирозиназы и TRP-1. Это наиболее «верхний» уровень регуляции — фактически перехват сигнала до того, как меланогенез вообще запущен.
Нетепловая плазма, включая аргоновые системы, действует на уровне редокс-химии: активирует Nrf2 → повышает внутриклеточный глутатион → перехватывает допахинон → переключает синтез с эумеланина на феомеланин и при достаточных концентрациях GSH модулирует активный сайт тирозиназы. Это «нижний» уровень регуляции — вмешательство непосредственно в химию меланинового синтеза.
Азотная плазма подтверждает клиническую эффективность в отношении рефрактерной мелазмы, а экспериментальные данные указывают на возможное влияние плазменных факторов на тирозиназу и связанные сигнальные пути.
Таким образом, холодная плазма может воздействовать на меланогенез на нескольких уровнях — от регуляции сигнальных путей до изменения редокс-среды. Однако степень доказанности этих механизмов различается: часть из них подтверждена на клеточных моделях, часть — на клинических наблюдениях, и требует дальнейшей верификации в контролируемых исследованиях.
Аргоновая плазма действует на уровне гормонального рецептора и транскрипционного контроля: подавляет YAP в меланоцитах → снижает MC1R → ослабляет α-МСГ-зависимую активацию PKA/CREB/MITF → уменьшает экспрессию тирозиназы и TRP-1. Это наиболее «верхний» уровень регуляции — фактически перехват сигнала до того, как меланогенез вообще запущен.
Нетепловая плазма, включая аргоновые системы, действует на уровне редокс-химии: активирует Nrf2 → повышает внутриклеточный глутатион → перехватывает допахинон → переключает синтез с эумеланина на феомеланин и при достаточных концентрациях GSH модулирует активный сайт тирозиназы. Это «нижний» уровень регуляции — вмешательство непосредственно в химию меланинового синтеза.
Азотная плазма подтверждает клиническую эффективность в отношении рефрактерной мелазмы, а экспериментальные данные указывают на возможное влияние плазменных факторов на тирозиназу и связанные сигнальные пути.
Таким образом, холодная плазма может воздействовать на меланогенез на нескольких уровнях — от регуляции сигнальных путей до изменения редокс-среды. Однако степень доказанности этих механизмов различается: часть из них подтверждена на клеточных моделях, часть — на клинических наблюдениях, и требует дальнейшей верификации в контролируемых исследованиях.
Источники
[1] Kim HY, Agrahari G, Lee MJ et al. Low-Temperature Argon Plasma Regulates Skin Moisturizing and Melanogenesis-Regulating Markers through Yes-Associated Protein. Int J Mol Sci. 2021;22(4):1895. PMID: 33672928.
[2] Schmidt A, Dietrich S, Steuer A et al. Non-thermal Plasma Activates Human Keratinocytes by Stimulation of Antioxidant and Phase II Pathways. J Biol Chem. 2015;290(11):6731–6750. PMID: 25589789.
[3] Villarama CD, Maibach HI. Glutathione as a depigmenting agent: an overview. Int J Cosmet Sci. 2005;27(3):147–153. PMID: 18492181.
[4] Jara JR, Aroca P, Solano F et al. The role of sulfhydryl compounds in mammalian melanogenesis: the effect of cysteine and glutathione upon tyrosinase and the intermediates of the pathway. Biochim Biophys Acta. 1988;967(2):296–303. PMID: 2903772.
[5] Kim HJ, Kim H, Kim YK et al. Treatment of Refractory Melasma with Microwave-generated, Atmospheric-pressure, Non-thermal Nitrogen Plasma. Med Lasers. 2019;8(2):74–79. DOI: 10.25289/ML.2019.8.2.74.
[6] Ali A, Kim YH, Kim TH et al. Influence of plasma-activated compounds on melanogenesis and tyrosinase activity. Sci Rep. 2016;6:21779. DOI: 10.1038/srep21779
[2] Schmidt A, Dietrich S, Steuer A et al. Non-thermal Plasma Activates Human Keratinocytes by Stimulation of Antioxidant and Phase II Pathways. J Biol Chem. 2015;290(11):6731–6750. PMID: 25589789.
[3] Villarama CD, Maibach HI. Glutathione as a depigmenting agent: an overview. Int J Cosmet Sci. 2005;27(3):147–153. PMID: 18492181.
[4] Jara JR, Aroca P, Solano F et al. The role of sulfhydryl compounds in mammalian melanogenesis: the effect of cysteine and glutathione upon tyrosinase and the intermediates of the pathway. Biochim Biophys Acta. 1988;967(2):296–303. PMID: 2903772.
[5] Kim HJ, Kim H, Kim YK et al. Treatment of Refractory Melasma with Microwave-generated, Atmospheric-pressure, Non-thermal Nitrogen Plasma. Med Lasers. 2019;8(2):74–79. DOI: 10.25289/ML.2019.8.2.74.
[6] Ali A, Kim YH, Kim TH et al. Influence of plasma-activated compounds on melanogenesis and tyrosinase activity. Sci Rep. 2016;6:21779. DOI: 10.1038/srep21779
09
Механизм 7. Нормализация микроциркуляции и устранение стаза
Оксид азота — один из ключевых регуляторов заживления кожи. Снижение его биодоступности нарушает микроциркуляцию и замедляет репаративные процессы. Холодная атмосферная плазма компенсирует это за счёт генерации реактивных форм азота, которые формируют NO-зависимый сигнальный ответ в тканях — не как прямой источник готового NO, а как триггер собственных клеточных механизмов [1, 5].
Сосудистый эффект. NO регулирует тонус сосудов через активацию растворимой гуанилатциклазы: рост цГМФ расслабляет гладкомышечные клетки сосудистой стенки, расширяет просвет сосуда и улучшает тканевую перфузию [1]. В экспериментальной модели ожога плазменное воздействие модулировало активность эндотелиальной NO-синтазы и усиливало неоваскуляризацию в раневой ткани, что сопровождалось ускорением репарации [2].
Клеточные эффекты. NO участвует в регуляции клеточного поведения на всех ключевых этапах заживления [3, 4]. В фазе воспаления он модулирует активность иммунных клеток и ограничивает избыточный воспалительный ответ. В фазе пролиферации стимулирует миграцию и деление кератиноцитов, ускоряя закрытие раны, и активирует фибробласты, усиливая синтез коллагена и внеклеточного матрикса [3, 4, 6]. В фазе ремоделирования участвует в регуляции баланса между синтезом и деградацией матрикса, влияя на конечное качество рубца.
Ангиогенез. NO — один из ключевых проангиогенных сигналов: он участвует в активации эндотелиальных клеток, их пролиферации и формировании новых капилляров. Восстановление капиллярной сети в зоне повреждения критически важно для долгосрочного питания ткани и её функционального восстановления [2, 5].
Таким образом, через реактивные формы азота и редокс-сигналинг плазменное воздействие затрагивает сразу несколько уровней репаративного процесса: улучшает микроциркуляцию, поддерживает клеточную активность на всех фазах заживления и стимулирует формирование новых сосудов в восстанавливающейся ткани [2, 5, 6].
Сосудистый эффект. NO регулирует тонус сосудов через активацию растворимой гуанилатциклазы: рост цГМФ расслабляет гладкомышечные клетки сосудистой стенки, расширяет просвет сосуда и улучшает тканевую перфузию [1]. В экспериментальной модели ожога плазменное воздействие модулировало активность эндотелиальной NO-синтазы и усиливало неоваскуляризацию в раневой ткани, что сопровождалось ускорением репарации [2].
Клеточные эффекты. NO участвует в регуляции клеточного поведения на всех ключевых этапах заживления [3, 4]. В фазе воспаления он модулирует активность иммунных клеток и ограничивает избыточный воспалительный ответ. В фазе пролиферации стимулирует миграцию и деление кератиноцитов, ускоряя закрытие раны, и активирует фибробласты, усиливая синтез коллагена и внеклеточного матрикса [3, 4, 6]. В фазе ремоделирования участвует в регуляции баланса между синтезом и деградацией матрикса, влияя на конечное качество рубца.
Ангиогенез. NO — один из ключевых проангиогенных сигналов: он участвует в активации эндотелиальных клеток, их пролиферации и формировании новых капилляров. Восстановление капиллярной сети в зоне повреждения критически важно для долгосрочного питания ткани и её функционального восстановления [2, 5].
Таким образом, через реактивные формы азота и редокс-сигналинг плазменное воздействие затрагивает сразу несколько уровней репаративного процесса: улучшает микроциркуляцию, поддерживает клеточную активность на всех фазах заживления и стимулирует формирование новых сосудов в восстанавливающейся ткани [2, 5, 6].
Источники
[1] Tsoukias NM, Kavdia M, Popel AS. Nitric Oxide Signaling in the Microcirculation. Microcirculation. 2013.
[2] Duchesne C, Banzet S, Lataillade JJ, Rousseau A, Frescaline N. Cold atmospheric plasma modulates endothelial nitric oxide synthase signalling and enhances burn wound neovascularisation. J Pathol. 2019;249(3):368–380. PMID: 31265742.
[3] Luo JD, Chen AF. Nitric oxide: a newly discovered function on wound healing. Acta Pharmacol Sin. 2005;26:259–264.
[4] Schäffer MR, Efron PA, Thornton FJ, Klingel K, Gross SS, Barbul A. Nitric oxide, an autocrine regulator of wound fibroblast synthetic function. J Immunol. 1997;158(5):2375–2381. PMID: 9036987.
[5] Zhai SY, Kong MG, Xia YM. Cold Atmospheric Plasma Ameliorates Skin Diseases Involving Reactive Oxygen/Nitrogen Species-Mediated Functions. Front Immunol. 2022;13:868386. PMID: 35720416.
[6] Brun P, Pathak S, Castagliuolo I et al. Cold Atmospheric Plasma Jet Treatment Improves Human Keratinocyte Migration and Wound Closure Capacity without Causing Cellular Oxidative Stress. Int J Mol Sci. 2022;23(18):10650.
[2] Duchesne C, Banzet S, Lataillade JJ, Rousseau A, Frescaline N. Cold atmospheric plasma modulates endothelial nitric oxide synthase signalling and enhances burn wound neovascularisation. J Pathol. 2019;249(3):368–380. PMID: 31265742.
[3] Luo JD, Chen AF. Nitric oxide: a newly discovered function on wound healing. Acta Pharmacol Sin. 2005;26:259–264.
[4] Schäffer MR, Efron PA, Thornton FJ, Klingel K, Gross SS, Barbul A. Nitric oxide, an autocrine regulator of wound fibroblast synthetic function. J Immunol. 1997;158(5):2375–2381. PMID: 9036987.
[5] Zhai SY, Kong MG, Xia YM. Cold Atmospheric Plasma Ameliorates Skin Diseases Involving Reactive Oxygen/Nitrogen Species-Mediated Functions. Front Immunol. 2022;13:868386. PMID: 35720416.
[6] Brun P, Pathak S, Castagliuolo I et al. Cold Atmospheric Plasma Jet Treatment Improves Human Keratinocyte Migration and Wound Closure Capacity without Causing Cellular Oxidative Stress. Int J Mol Sci. 2022;23(18):10650.
10
Механизм 8. Себорегуляция через ядерные рецепторы
Холодная атмосферная плазма влияет на работу сальных желёз на клеточном уровне. В экспериментах на животных аргоновая плазма вызывала структурные изменения в себоцитах — клетках, вырабатывающих кожное сало, — не повреждая при этом окружающие ткани, что указывает на избирательное воздействие именно на клетки сальных желёз [1].
Эти данные получили подтверждение в двух клинических исследованиях с непосредственным участием PLADUO. В первом, рандомизированном исследовании на 15 добровольцах с жирным типом кожи, три процедуры с аргоновой и азотной плазмой снизили уровень кожного сала на 22−28% к четвёртой неделе. Индекс порфиринов — маркер активности C. acnes в порах — упал на 28−38% уже на второй неделе. Гистологический анализ биоптатов не выявил термического повреждения кожи, побочные эффекты ограничились временным покраснением [2]. Во втором проспективном исследовании на 24 пациентах с акне I-III степени тяжести и фототипами I-IV курс терапии PLADUO продолжительностью три месяца показал положительную динамику у 62,5% пациентов, успешно завершивших лечение. Исследование дополнительно выявило накопительный эффект: у 100% пациентов улучшение продолжалось в течение месячного перерыва между процедурами [3].
На молекулярном уровне оба типа плазмы подавляют синтез липидов в себоцитах — в том числе стимулированный андрогенами и жирными кислотами. Ключевой мишенью служит PPARγ — белок, управляющий созреванием себоцитов и запускающий программу выработки кожного сала. После плазменного воздействия его экспрессия снижается, что тормозит дифференцировку клеток и синтез липидов. Параллельно снижается пролиферация себоцитов: маркер деления клеток Ki67 в базальном слое сальных желёз достоверно уменьшался после курса процедур — без признаков апоптоза [1, 2].
Это принципиально отличает плазму от большинства топических средств против акне: воздействие направлено не на устранение симптомов, а на патогенетические механизмы — дифференцировку клеток сальных желёз и синтез липидов, лежащие в основе гиперсебореи [1, 2, 3].
Эти данные получили подтверждение в двух клинических исследованиях с непосредственным участием PLADUO. В первом, рандомизированном исследовании на 15 добровольцах с жирным типом кожи, три процедуры с аргоновой и азотной плазмой снизили уровень кожного сала на 22−28% к четвёртой неделе. Индекс порфиринов — маркер активности C. acnes в порах — упал на 28−38% уже на второй неделе. Гистологический анализ биоптатов не выявил термического повреждения кожи, побочные эффекты ограничились временным покраснением [2]. Во втором проспективном исследовании на 24 пациентах с акне I-III степени тяжести и фототипами I-IV курс терапии PLADUO продолжительностью три месяца показал положительную динамику у 62,5% пациентов, успешно завершивших лечение. Исследование дополнительно выявило накопительный эффект: у 100% пациентов улучшение продолжалось в течение месячного перерыва между процедурами [3].
На молекулярном уровне оба типа плазмы подавляют синтез липидов в себоцитах — в том числе стимулированный андрогенами и жирными кислотами. Ключевой мишенью служит PPARγ — белок, управляющий созреванием себоцитов и запускающий программу выработки кожного сала. После плазменного воздействия его экспрессия снижается, что тормозит дифференцировку клеток и синтез липидов. Параллельно снижается пролиферация себоцитов: маркер деления клеток Ki67 в базальном слое сальных желёз достоверно уменьшался после курса процедур — без признаков апоптоза [1, 2].
Это принципиально отличает плазму от большинства топических средств против акне: воздействие направлено не на устранение симптомов, а на патогенетические механизмы — дифференцировку клеток сальных желёз и синтез липидов, лежащие в основе гиперсебореи [1, 2, 3].
Источники
[1] Kim H, Kim HJ, Kim HK, Hong JY, Cho SB. Effects of argon and nitrogen plasma pulses on the skin and skin appendages in an in vivo animal model. Skin Res Technol. 2020;26(1):81−90. PMID: 31 532 008. Источник на сайте PLADUO: https://pladuo.ru/argonandnitrogenplasma
[2] Kim SE, Lee SE, Cho SB et al. Argon- and nitrogen-plasma pulses decrease facial sebum excretion in oily human skin by regulating lipogenesis and proliferation in human sebocytes. ClinicalTrials.gov: NCT04917835. Research Square. 2021. DOI: 10.21 203/rs.3.rs-729 953/v1. Источник на сайте PLADUO: https://pladuo.ru/plasmapulses
[3] Клиническое исследование терапии акне холодной плазмой. Отчёт о клинических испытаниях: обзор и результаты. Проспективное интервенционное исследование, n=24, 2024. Источник на сайте PLADUO: https://pladuo.ru/therapy-for-acne
[2] Kim SE, Lee SE, Cho SB et al. Argon- and nitrogen-plasma pulses decrease facial sebum excretion in oily human skin by regulating lipogenesis and proliferation in human sebocytes. ClinicalTrials.gov: NCT04917835. Research Square. 2021. DOI: 10.21 203/rs.3.rs-729 953/v1. Источник на сайте PLADUO: https://pladuo.ru/plasmapulses
[3] Клиническое исследование терапии акне холодной плазмой. Отчёт о клинических испытаниях: обзор и результаты. Проспективное интервенционное исследование, n=24, 2024. Источник на сайте PLADUO: https://pladuo.ru/therapy-for-acne
11
Механизм 9. Широкоспектральная антибактериальная и антикандидная защита без резистентности
Холодная атмосферная плазма (ХАП) обладает широкоспектральной противомикробной активностью в отношении клинически значимых патогенов кожи. Механизм действия основан на генерации активных форм кислорода (ROS) и азота (RNS), которые повреждают липидный бислой бактериальных мембран, нарушают структуру белков и вызывают одно- и двуцепочечные разрывы ДНК патогенов [1, 2]. В отличие от антибиотиков, данный механизм является физическим и многокомпонентным, что исключает возможность формирования резистентности.

Спектр противомикробной активности ХАП включает грамотрицательные бактерии (E. coli, K. pneumoniae, P. aeruginosa), грамположительные микроорганизмы (S. aureus, MRSA), C. acnes — ключевой патоген в патогенезе акне — а также грибы рода Candida [1]. Аргоновая плазма реализует преимущественно ROS-зависимый путь деструкции через генерацию гидроксильных радикалов и супероксида; азотная плазма дополняет этот механизм пероксинитритным RNS-путём. При комбинированном воздействии N₂/Ar оба пути работают аддитивно, обеспечивая более широкое перекрытие спектра патогенов [1, 2].
Противогрибковая активность ХАП имеет самостоятельное клиническое значение. В клиническом отчёте с использованием PLADUO описан случай успешного лечения дерматофитии стоп, резистентной к системному итраконазолу и наружному эконазолу: два сеанса низкоэнергетической азотной плазмы (0,75 Дж/импульс, 7 мс, 2,45 ГГц, 2 прохода) привели к полному клиническому разрешению в течение двух недель с отрицательным результатом теста с КОН через месяц после последней процедуры. Болевые ощущения были минимальными, период восстановления не требовался, побочные эффекты ограничились лёгким ощущением тепла [3]. Механизм противогрибкового действия связывается с прямым повреждением грибковых гиф и спор в роговом слое и верхних слоях эпидермиса вследствие энергозависимой термической реакции в этих слоях без повреждения подлежащей дермальной стромы [3].
Существенным клиническим преимуществом ХАП является отсутствие системной токсичности, характерной для традиционных противогрибковых препаратов — в частности, гепатотоксичности, нарушений ферментативной функции печени и лекарственных взаимодействий, ограничивающих применение системных антимикотиков. Это делает плазменную терапию перспективной как в качестве монотерапии резистентных форм, так и в составе комбинированных протоколов [3].
Противогрибковая активность ХАП имеет самостоятельное клиническое значение. В клиническом отчёте с использованием PLADUO описан случай успешного лечения дерматофитии стоп, резистентной к системному итраконазолу и наружному эконазолу: два сеанса низкоэнергетической азотной плазмы (0,75 Дж/импульс, 7 мс, 2,45 ГГц, 2 прохода) привели к полному клиническому разрешению в течение двух недель с отрицательным результатом теста с КОН через месяц после последней процедуры. Болевые ощущения были минимальными, период восстановления не требовался, побочные эффекты ограничились лёгким ощущением тепла [3]. Механизм противогрибкового действия связывается с прямым повреждением грибковых гиф и спор в роговом слое и верхних слоях эпидермиса вследствие энергозависимой термической реакции в этих слоях без повреждения подлежащей дермальной стромы [3].
Существенным клиническим преимуществом ХАП является отсутствие системной токсичности, характерной для традиционных противогрибковых препаратов — в частности, гепатотоксичности, нарушений ферментативной функции печени и лекарственных взаимодействий, ограничивающих применение системных антимикотиков. Это делает плазменную терапию перспективной как в качестве монотерапии резистентных форм, так и в составе комбинированных протоколов [3].
Источники
[1] Kim CK, Kim H, Kim HJ, Cho SB. Antibacterial and anticandidal effects of atmospheric-pressure, non-thermal, nitrogen- and argon-plasma pulses. Dermatol Ther. 2022;35(2):e15222. DOI: 10.1111/dth.15 222. Источник на сайте PLADUO: https://pladuo.ru/anti-candidaaction
[2] Kim H, Kim HJ, Kim HK, Hong JY, Cho SB. Effects of argon and nitrogen plasma pulses on the skin and skin appendages in an in vivo animal model. Skin Res Technol. 2020;26(1):81−90. PMID: 31 532 008. Источник на сайте PLADUO: https://pladuo.ru/argonandnitrogenplasma
[3] Kim H, Cho SB, Kim HJ. Therapeutic Effect of Low-Energy Nitrogen Plasma Pulses on Tinea Pedis. J Korean Soc Laser Med Surg. 2019. (Клинический случай с использованием PLADUO™, SHEnB Co., Ltd., Сеул, Южная Корея.) Источник на сайте PLADUO: https://pladuo.ru/effect-of-low-energy
[2] Kim H, Kim HJ, Kim HK, Hong JY, Cho SB. Effects of argon and nitrogen plasma pulses on the skin and skin appendages in an in vivo animal model. Skin Res Technol. 2020;26(1):81−90. PMID: 31 532 008. Источник на сайте PLADUO: https://pladuo.ru/argonandnitrogenplasma
[3] Kim H, Cho SB, Kim HJ. Therapeutic Effect of Low-Energy Nitrogen Plasma Pulses on Tinea Pedis. J Korean Soc Laser Med Surg. 2019. (Клинический случай с использованием PLADUO™, SHEnB Co., Ltd., Сеул, Южная Корея.) Источник на сайте PLADUO: https://pladuo.ru/effect-of-low-energy
12
Механизм 10. Кальциевый ответ как раннее звено плазменного воздействия
Кальций рассматривается как один из ранних внутриклеточных медиаторов ответа на холодную атмосферную плазму. Плазменное воздействие создаёт на поверхности клетки комплексный физико-химический стимул, включающий реактивные формы кислорода и азота, локальные изменения окислительно-восстановительной среды и мембранные эффекты. В ответ на это в клетках может быстро возрастать концентрация Ca²⁺ в цитозоле, что рассматривается как один из механизмов перевода внешнего плазменного сигнала во внутриклеточный биологический ответ [1,6].
Экспериментальные данные показывают, что ХАП способна вызывать кальциевый ответ в клетках, а сам Ca²⁺ выступает функционально значимым звеном между плазменным стимулом и последующими клеточными изменениями [1,2]. Для кожи это особенно важно, поскольку кальций играет ключевую роль в регуляции эпидермального гомеостаза: участвует в переключении кератиноцитов от пролиферации к дифференцировке, в формировании барьерной функции и в восстановлении после повреждения [4,5].
Экспериментальные данные показывают, что ХАП способна вызывать кальциевый ответ в клетках, а сам Ca²⁺ выступает функционально значимым звеном между плазменным стимулом и последующими клеточными изменениями [1,2]. Для кожи это особенно важно, поскольку кальций играет ключевую роль в регуляции эпидермального гомеостаза: участвует в переключении кератиноцитов от пролиферации к дифференцировке, в формировании барьерной функции и в восстановлении после повреждения [4,5].
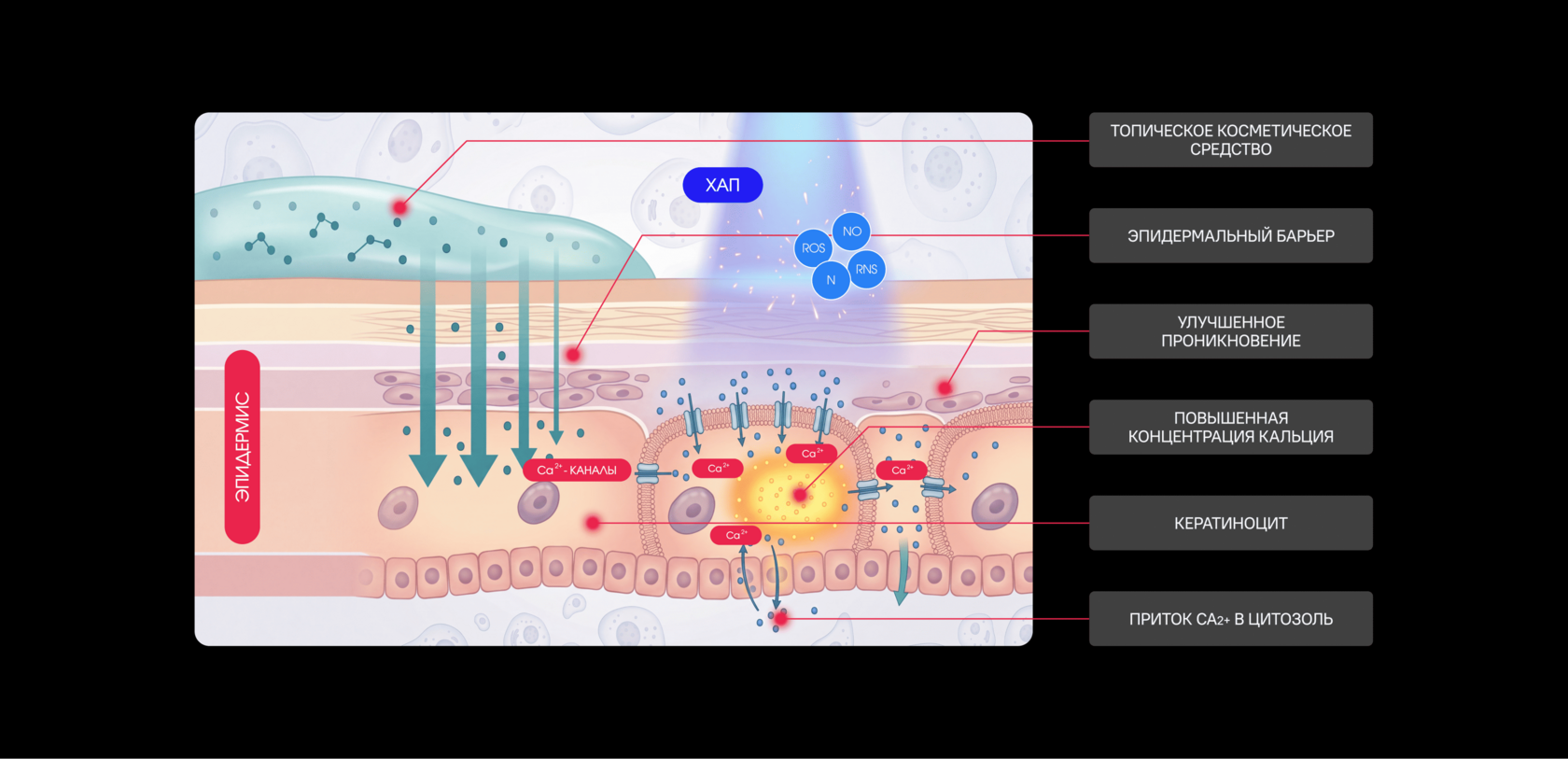
Подтверждение этой связи получено и в кожных моделях холодной атмосферной плазмы. В работе, посвящённой противовоспалительному плазменному пластырю, показано, что такое воздействие сопровождалось кальциевым ответом в кератиноцитах и ассоциировалось с восстановлением нарушенной дифференцировки и барьерной функции [3]. Это позволяет рассматривать кальциевый ответ как один из вероятных механизмов, через которые плазма влияет на состояние эпидермиса.
Практически это важно и в контексте сочетания с топическими средствами. Если плазменное воздействие временно меняет функциональное состояние клеток кожи, включая процессы дифференцировки, барьерной регуляции и клеточного ответа на стресс, то последующее нанесение наружных средств потенциально может давать более выраженный эффект. В первую очередь это касается противовоспалительных, восстанавливающих и депигментирующих формул. Таким образом, кальциевый ответ можно рассматривать как один из механизмов, который делает кожу более биологически восприимчивой к последующей наружной терапии, хотя конкретные схемы сочетания ещё требуют дальнейшего изучения.
Таким образом, холодная атмосферная плазма может рассматриваться как внешний физико-химический стимул, который преобразуется в тканевый ответ через кальциевую сигнализацию. Это делает Ca²⁺ важным звеном, связывающим плазменное воздействие с регуляцией дифференцировки эпидермиса, барьерной функции, митохондриального состояния и клеточной адаптации [1−3,6].
Практически это важно и в контексте сочетания с топическими средствами. Если плазменное воздействие временно меняет функциональное состояние клеток кожи, включая процессы дифференцировки, барьерной регуляции и клеточного ответа на стресс, то последующее нанесение наружных средств потенциально может давать более выраженный эффект. В первую очередь это касается противовоспалительных, восстанавливающих и депигментирующих формул. Таким образом, кальциевый ответ можно рассматривать как один из механизмов, который делает кожу более биологически восприимчивой к последующей наружной терапии, хотя конкретные схемы сочетания ещё требуют дальнейшего изучения.
Таким образом, холодная атмосферная плазма может рассматриваться как внешний физико-химический стимул, который преобразуется в тканевый ответ через кальциевую сигнализацию. Это делает Ca²⁺ важным звеном, связывающим плазменное воздействие с регуляцией дифференцировки эпидермиса, барьерной функции, митохондриального состояния и клеточной адаптации [1−3,6].
Источники
[1] Schneider C, Gebhardt L, Arndt S et al. Cold atmospheric plasma causes a calcium influx in melanoma cells triggering CAP-induced senescence. Scientific Reports, 2018. www.nature.com/articles
[2] Iuchi K et al. Cold atmospheric-pressure nitrogen plasma induces the production of reactive nitrogen species and cell death by increasing intracellular calcium in HEK293T cells. Archives of Biochemistry and Biophysics, 2018. www.pubmed.ncbi.nlm.nih.gov
[3] Iuchi K et al. Cold atmospheric nitrogen plasma induces metal-initiated cell death by cell membrane rupture and mitochondrial perturbation. Cell Biochemistry and Function, 2023. www.pubmed.ncbi.nlm.nih.gov
[4] Kim N et al. Portable Cold Atmospheric Plasma Patch-Mediated Skin Anti-Inflammatory Therapy. Advanced Science, 2022. www.advanced.onlinelibrary.wiley.com
[5] Bikle DD, Xie Z, Tu CL. Calcium regulation of keratinocyte differentiation. Expert Review of Endocrinology & Metabolism, 2012. www.pubmed.ncbi.nlm.nih.gov
[6] Lee SE, Lee SH. Skin Barrier and Calcium. Annals of Dermatology, 2018. www.pubmed.ncbi.nlm.nih.gov
[2] Iuchi K et al. Cold atmospheric-pressure nitrogen plasma induces the production of reactive nitrogen species and cell death by increasing intracellular calcium in HEK293T cells. Archives of Biochemistry and Biophysics, 2018. www.pubmed.ncbi.nlm.nih.gov
[3] Iuchi K et al. Cold atmospheric nitrogen plasma induces metal-initiated cell death by cell membrane rupture and mitochondrial perturbation. Cell Biochemistry and Function, 2023. www.pubmed.ncbi.nlm.nih.gov
[4] Kim N et al. Portable Cold Atmospheric Plasma Patch-Mediated Skin Anti-Inflammatory Therapy. Advanced Science, 2022. www.advanced.onlinelibrary.wiley.com
[5] Bikle DD, Xie Z, Tu CL. Calcium regulation of keratinocyte differentiation. Expert Review of Endocrinology & Metabolism, 2012. www.pubmed.ncbi.nlm.nih.gov
[6] Lee SE, Lee SH. Skin Barrier and Calcium. Annals of Dermatology, 2018. www.pubmed.ncbi.nlm.nih.gov
13
Наука в руках врача — бесконечный потенциал для тех, кто работает с доказательствами
Холодная атмосферная плазма — один из немногих физических методов, для которых одновременно задокументировано воздействие на несколько фундаментальных механизмов старения кожи: редокс-дисбаланс, хроническое воспаление, деградацию матрикса, нарушение барьерной функции, дисрегуляцию пигментации и микроциркуляторный стаз. Каждый из девяти описанных механизмов опирается на конкретные молекулярные мишени — от Nrf2 и NF-κB до YAP, MITF, PPARγ и эндотелиальной NO-синтазы — и подтверждён в экспериментальных или клинических исследованиях.
Принципиально важно, что всё это достигается локально, без системного введения препаратов, без накопления метаболитов и без риска лекарственных взаимодействий. Плазма не добавляет в организм ничего чужеродного — она активирует собственные клеточные программы: антиоксидантную защиту, синтез матрикса, барьерные белки, сосудистый ответ. Тело делает работу само — плазма лишь задаёт правильный сигнал.
Для врача, работающего с доказательной базой, это означает следующее: в одном физическом воздействии сосредоточен потенциал, который в фармакологии потребовал бы комбинации из шести и более препаратов — с соответствующей нагрузкой на пациента. Здесь этой нагрузки нет. Есть молекулярная точность, клиническая управляемость и растущий массив данных, который продолжает расширяться по мере того, как технология переходит из лабораторий в клиническую практику.
Принципиально важно, что всё это достигается локально, без системного введения препаратов, без накопления метаболитов и без риска лекарственных взаимодействий. Плазма не добавляет в организм ничего чужеродного — она активирует собственные клеточные программы: антиоксидантную защиту, синтез матрикса, барьерные белки, сосудистый ответ. Тело делает работу само — плазма лишь задаёт правильный сигнал.
Для врача, работающего с доказательной базой, это означает следующее: в одном физическом воздействии сосредоточен потенциал, который в фармакологии потребовал бы комбинации из шести и более препаратов — с соответствующей нагрузкой на пациента. Здесь этой нагрузки нет. Есть молекулярная точность, клиническая управляемость и растущий массив данных, который продолжает расширяться по мере того, как технология переходит из лабораторий в клиническую практику.
Читайте статьи:
30 Июня 2024
Новые технологии красоты


30 Июня 2024
Новые технологии красоты


30 Июня 2024
Новые технологии красоты


Все статьи из блога
Все статьи из блога









