

Оставить заявку
Оставить заявку

ОСТАВИТЬ ЗАЯВКУ
Заполняя данную форму, вы соглашаетесь с Правилами обработки персональных данных
Влияние низкотемпературной аргоновой плазмы на ремоделирование внеклеточного матрикса гипертрофического рубца кожи: гистологическое и иммуногистохимическое исследование.
11 Марта 2026

Новые технологии красоты

Авторы: О.Ф. Соколова, А.А. Веревкин. Кубанский государственный медицинский университет, Краснодар, Россия
01
Аннотация
Цель: Оценка гистологических изменений и динамики экспрессии коллагена III типа в рубцовой ткани кожи человека после двукратного воздействия низкотемпературной аргоновой плазмой.
Материалы и методы: В качестве объекта исследования использовали парные биоптаты кожи в области одного гипертрофического рубца, полученные до и после двух процедур воздействия. Гистологическое исследование проводили на срезах, окрашенных гематоксилином и эозином. Для иммуногистохимического исследования использовали поликлональные антитела к коллагену III типа и стрептавидин-пероксидазу с DAB-хромагеном. Для количественного анализа результатов иммунофенотипирования коллагены применили компьютерную морфометрию с определением коэффициента площади окрашивания — отношения площади иммунореактивного продукта к площади среза. Результаты представлены в виде медианы и интерквартильного размаха [Q1; Q3]. Для сопоставления выборочных значений в двух группах количественных признаков использовали критерий Манна-Уитни.
Результаты: Исходная группа образцов демонстрировала картину незрелого рубца: дезориентированные пучки грубоволокнистого коллагена, слабую диффузную лимфомакрофагальную инфильтрацию. Доля коллагена III типа составляла 4,7% [3,9; 5,6]. Группа образцов после воздействия характеризовалась восстановлением гистоархитектоники: исчезновение воспаления, появление пучков коллагена нормального строения и аморфного компонента, слабый акантоз эпидермиса. Объемная доля коллагена III типа статистически значимо возросла в 1,8 раза и достигла 8,4% [6,8; 9,9].
Заключение: Двукратная обработка низкотемпературной аргоновой плазмой индуцирует процессы активного ремоделирования рубцовой ткани, что морфологически проявляется купированием хронического воспаления, упорядочиванием коллагенового матрикса и сопровождается значительным увеличением доли коллагена III типа, маркера активного фибриллогенеза.
Ключевые слова: холодная плазма, аргон, гипертрофический рубец, ремоделирование, коллаген III типа, иммуногистохимия.
Материалы и методы: В качестве объекта исследования использовали парные биоптаты кожи в области одного гипертрофического рубца, полученные до и после двух процедур воздействия. Гистологическое исследование проводили на срезах, окрашенных гематоксилином и эозином. Для иммуногистохимического исследования использовали поликлональные антитела к коллагену III типа и стрептавидин-пероксидазу с DAB-хромагеном. Для количественного анализа результатов иммунофенотипирования коллагены применили компьютерную морфометрию с определением коэффициента площади окрашивания — отношения площади иммунореактивного продукта к площади среза. Результаты представлены в виде медианы и интерквартильного размаха [Q1; Q3]. Для сопоставления выборочных значений в двух группах количественных признаков использовали критерий Манна-Уитни.
Результаты: Исходная группа образцов демонстрировала картину незрелого рубца: дезориентированные пучки грубоволокнистого коллагена, слабую диффузную лимфомакрофагальную инфильтрацию. Доля коллагена III типа составляла 4,7% [3,9; 5,6]. Группа образцов после воздействия характеризовалась восстановлением гистоархитектоники: исчезновение воспаления, появление пучков коллагена нормального строения и аморфного компонента, слабый акантоз эпидермиса. Объемная доля коллагена III типа статистически значимо возросла в 1,8 раза и достигла 8,4% [6,8; 9,9].
Заключение: Двукратная обработка низкотемпературной аргоновой плазмой индуцирует процессы активного ремоделирования рубцовой ткани, что морфологически проявляется купированием хронического воспаления, упорядочиванием коллагенового матрикса и сопровождается значительным увеличением доли коллагена III типа, маркера активного фибриллогенеза.
Ключевые слова: холодная плазма, аргон, гипертрофический рубец, ремоделирование, коллаген III типа, иммуногистохимия.
02
Введение
Гипертрофические рубцы являются следствием нарушения физиологического процесса заживления ран, характеризующимся избыточным и неорганизованным отложением компонентов внеклеточного матрикса (ВКМ), главным образом коллагена I типа, на фоне персистирующего воспаления [1−3]. Грануляционная ткань, формирующаяся на раннем этапе пролиферации, содержит преиимущественно коллаген III типа, который является более мягким и занимает больший объем. По мере созревания рубца, он постепенно замещается жестким и менее объемным коллагеном I типа [4]. Современные физические методы коррекции, включая воздействие низкотемпературной плазмой (холодной плазмой), показывают клиническую эффективность в дерматологии и регенеративной медицине. Однако их влияние на патоморфоз и иммуногистохимический профиль, в частности, на баланс коллагеновых фибрилл, остается не до конца изученным.
03
Цель исследования
Проанализировать патоморфоз и изменение иммуногистохимического профиля внеклеточного матрикса рубцовой ткани на фоне курсового воздействия низкотемпературной аргоновой плазмой.
04
Материалы и методы
Объектом исследования послужил пациент 37 лет с послеоперационным рубцом в области голени. После получения информированного добровольного согласия у него была взята инцизионная биопсия кожи из области рубца. Затем пациенту выполнили две процедуры. воздействия холодной аргоновой плазмой (аппарат PLADUO, Республика Корея) в следующем режиме: мощность 0,63Дж, частота 3мГц, расстояние от аппликатора до поверхности кожи 5 мм, время экспозиции: на один сеанс — 60 секунд на площадь рубца 120 см². Время между процедурами составило 14 дней. Ппосле второго воздействия пациенту также была выполнена инцизионная биопсия. Биологический материал фиксировали в 10% нейтральном формалине (БиоВитрум, Россия), проводили через спирты и ксилол, заливали в парафин. Серийные срезы толщиной 4−5 мкм изготовили при помощи ротационного микротома RM2235 (Leica, ФРГ) и окрашивали гематоксилином (БиоВитрум, Россия) и эозином (Sigma-Aldrich, США) по стандартной методике [7].
Срезы для иммуногистохимического исследования помещали на стекла с поли-L-лизиновым покрытием (ThermoFischer Scientific, США). Для выявления коллагена III типа использовали поликлональные антитела (FRK21446, Cloud Clone, США). Для детектирования ИГХ-сигнала использовали DAB-хромаген и пероксидазу с стрептавидиновым усилением (Sigma-Aldrich, США). Протокол соответствовал рекомендациям производителя и общепринятым методикам [8]. Микроскопию и фотофиксацию проводили с использованием светового микроскопа Nikon E200 (Япония) и цифровой камеры MiCrome M16 (КНР).
Количественную оценку объемной доли коллагена III типа в дерме проводили с помощью коэффициента площади окрашивания (КПО) — отношения площади иммунореактивного продукта к площади среза. Для оценки использовалось программное обеспечение ImageJ (NIH, США). Анализировали не менее 10 случайных, не перекрывающихся полей зрения при увеличении x200 на каждом срезе. Результаты представлены в виде медианы (Me) и интерквартильного размаха [Q1; Q3].
Статистический анализ: Сравнение количественных показателей между группами «до» и «после» лечения проводили с использованием непараметрического критерия Уилкоксона для парных выборок в программе GraphPad Prism (GraphSoft, США). Различия считали статистически значимыми при p < 0.05.
Срезы для иммуногистохимического исследования помещали на стекла с поли-L-лизиновым покрытием (ThermoFischer Scientific, США). Для выявления коллагена III типа использовали поликлональные антитела (FRK21446, Cloud Clone, США). Для детектирования ИГХ-сигнала использовали DAB-хромаген и пероксидазу с стрептавидиновым усилением (Sigma-Aldrich, США). Протокол соответствовал рекомендациям производителя и общепринятым методикам [8]. Микроскопию и фотофиксацию проводили с использованием светового микроскопа Nikon E200 (Япония) и цифровой камеры MiCrome M16 (КНР).
Количественную оценку объемной доли коллагена III типа в дерме проводили с помощью коэффициента площади окрашивания (КПО) — отношения площади иммунореактивного продукта к площади среза. Для оценки использовалось программное обеспечение ImageJ (NIH, США). Анализировали не менее 10 случайных, не перекрывающихся полей зрения при увеличении x200 на каждом срезе. Результаты представлены в виде медианы (Me) и интерквартильного размаха [Q1; Q3].
Статистический анализ: Сравнение количественных показателей между группами «до» и «после» лечения проводили с использованием непараметрического критерия Уилкоксона для парных выборок в программе GraphPad Prism (GraphSoft, США). Различия считали статистически значимыми при p < 0.05.
05
Результаты и обсуждение
В группе до лечения дерма характеризовалась наличием грубоволокнистой соединительной ткани, что соответствовало незрелому гипертрофическому рубцу. Внеклеточный матрикс был представлен утолщенными, плотными, хаотично переплетенными и дезориентированными пучками коллагеновых волокон. В межволоконных пространствах определялась диффузная слабо выраженная инфильтрация, представленная лимфоцитами и макрофагами, что говорило о хроническом интерстициальном воспалении. При этом эпидермис имел нормальное строение.
В образцах из группы после двух процедур наблюдались выраженные признаки ремоделирования дермы. Грубые дезориентированные пучки коллагена замещались более тонкими, упорядоченными группами волокон, ориентированными параллельно поверхности кожи, что характерно для зрелой соединительной ткани. В матриксе появились участки аморфного слабо оксифильного основного вещества, что может соответствовать фазе активного обновления ВКМ. Топография таких фокусов реорганизации аморфного матрикса соответствовала периваскулярному пространству и зонам вокруг производных эпидермиса. Клеточная инфильтрация полностью отсутствовала. В эпидермисе отмечался слабо выраженный акантоз. Микрофотографии, демонстрирующие результаты гистологического анализа, представлены на рисунке 1.
В образцах из группы после двух процедур наблюдались выраженные признаки ремоделирования дермы. Грубые дезориентированные пучки коллагена замещались более тонкими, упорядоченными группами волокон, ориентированными параллельно поверхности кожи, что характерно для зрелой соединительной ткани. В матриксе появились участки аморфного слабо оксифильного основного вещества, что может соответствовать фазе активного обновления ВКМ. Топография таких фокусов реорганизации аморфного матрикса соответствовала периваскулярному пространству и зонам вокруг производных эпидермиса. Клеточная инфильтрация полностью отсутствовала. В эпидермисе отмечался слабо выраженный акантоз. Микрофотографии, демонстрирующие результаты гистологического анализа, представлены на рисунке 1.
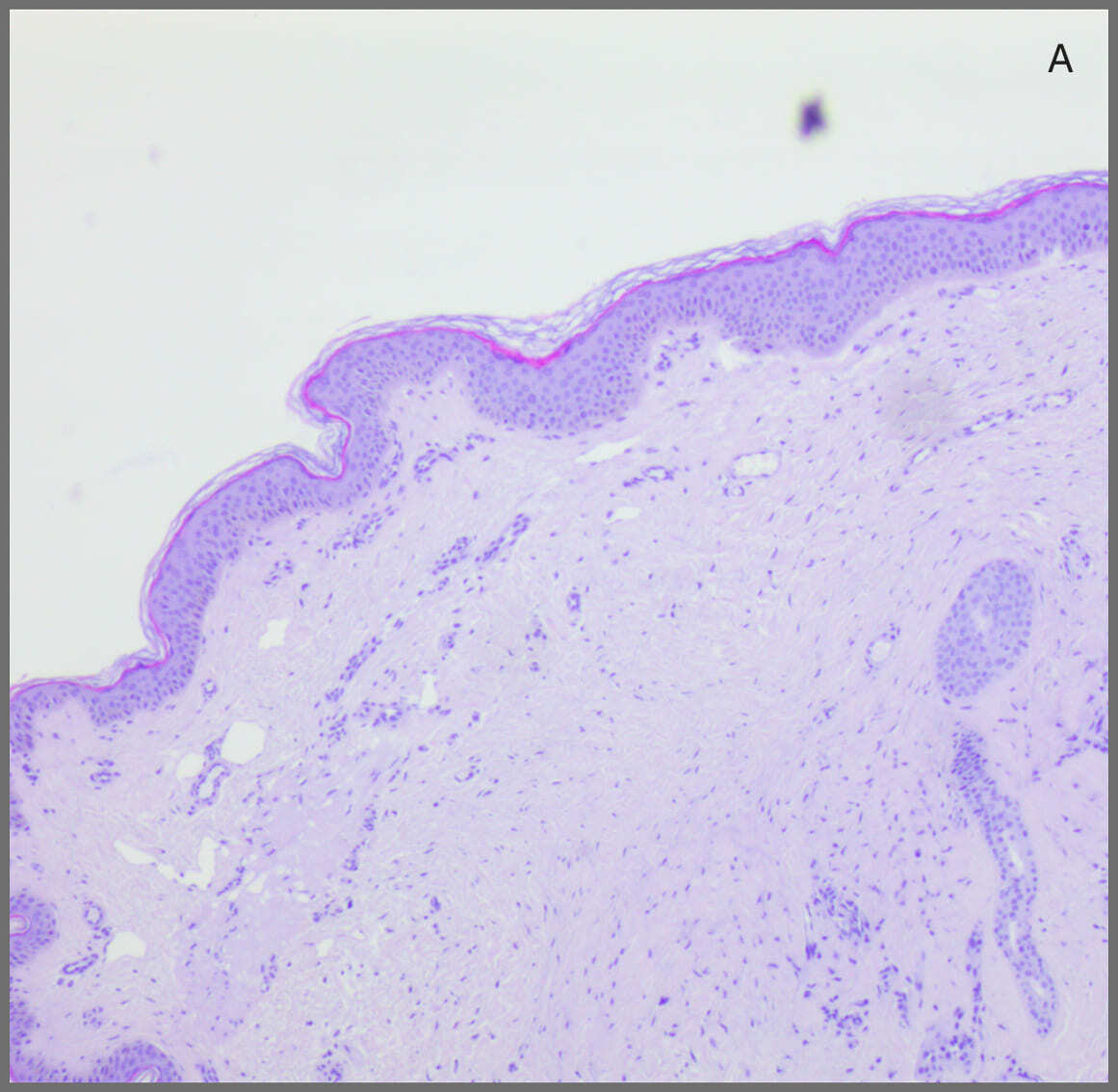
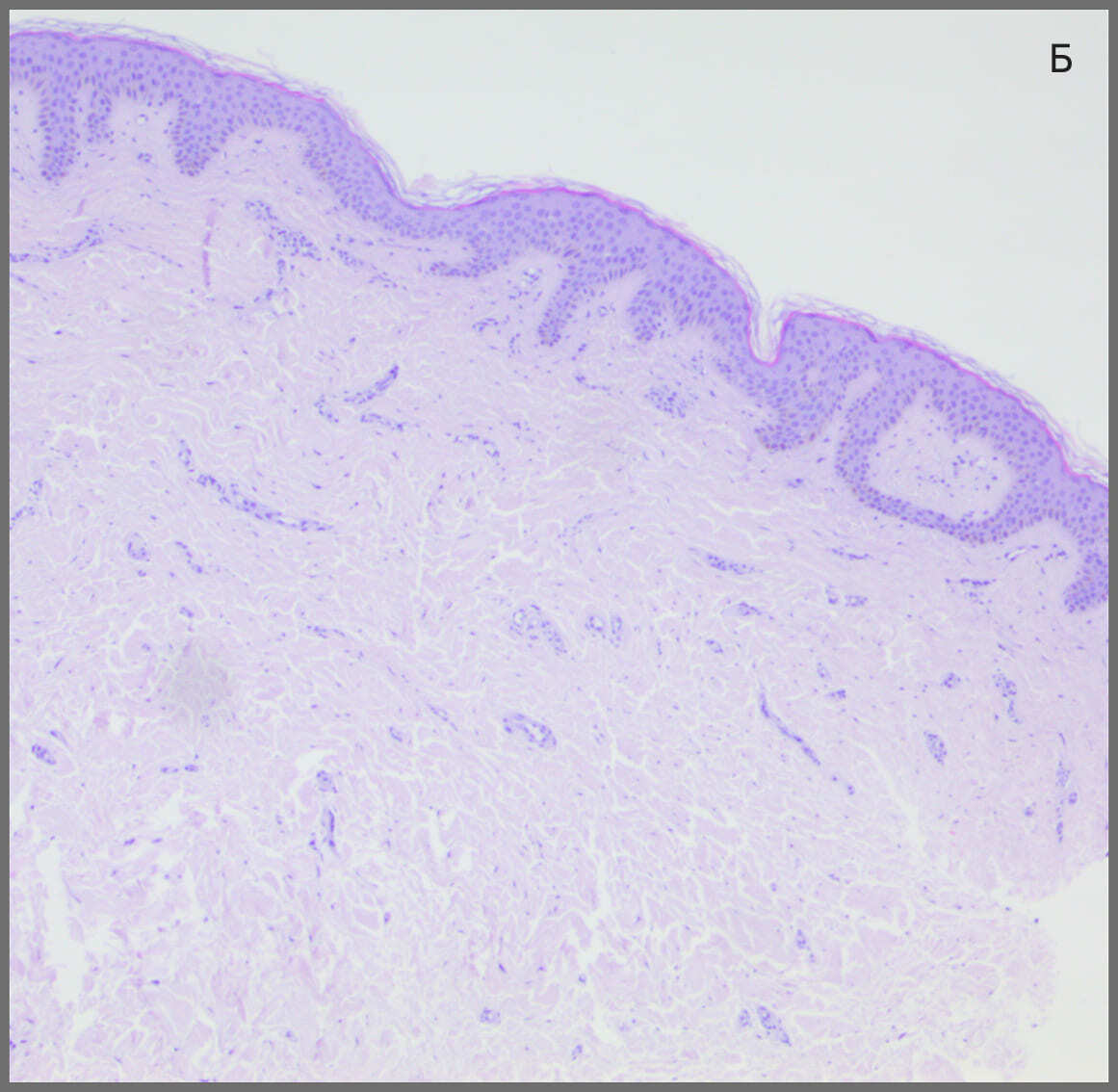
Рисунок 1. Результат гистологического анализа. А — образец до воздействия. Слабо выраженная лимфомакрофагальная инфильтрация, хаотично расположенные пучки коллагена. Б — образец после воздействия. Воспалительный инфильтрат отсутствует, коллаген нормального строения, слабо выраженный акантоз. Гематоксилин-эозин, увеличение х 10.
Иммуногистохимическая реакция на коллаген III типа в группе до лечения была слабоинтенсивной и рассеянной. После лечения интенсивность и площадь специфического окрашивания существенно увеличились, сигнал коррелировал с зонами реорганизации матрикса. Результат иммунотипирования коллагена III типа позволил установить, что большинство очагов неоколлагеногенеза приходится на периваскулярное пространство. Микрофотографии препаратов, подвергнутых иммуногистохимическому анализу, представлены на рисунке 2.
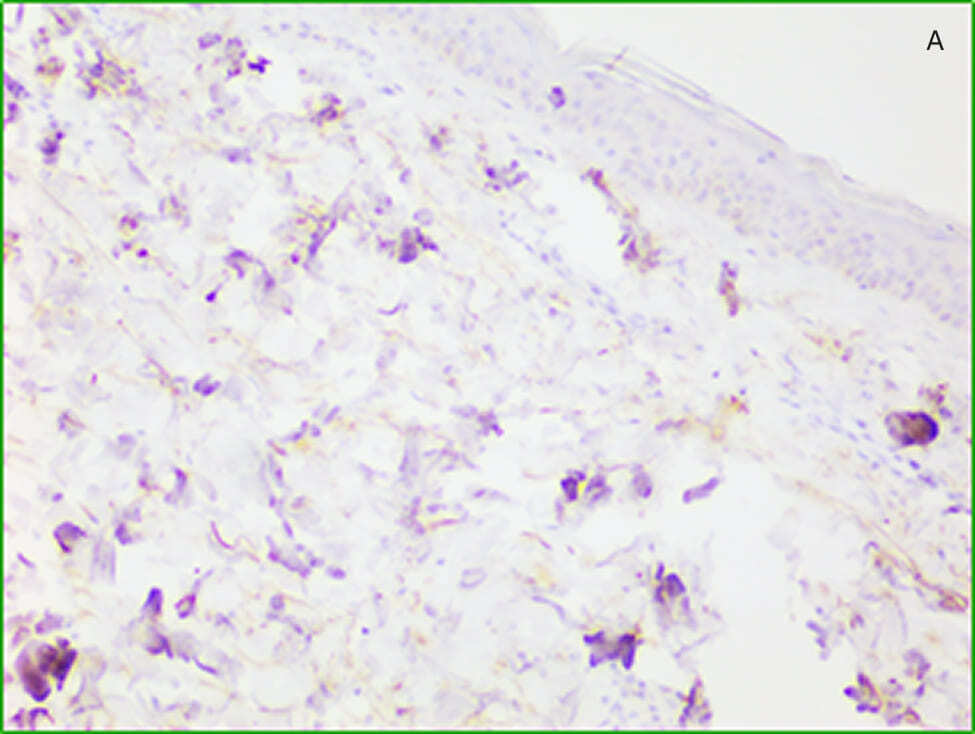
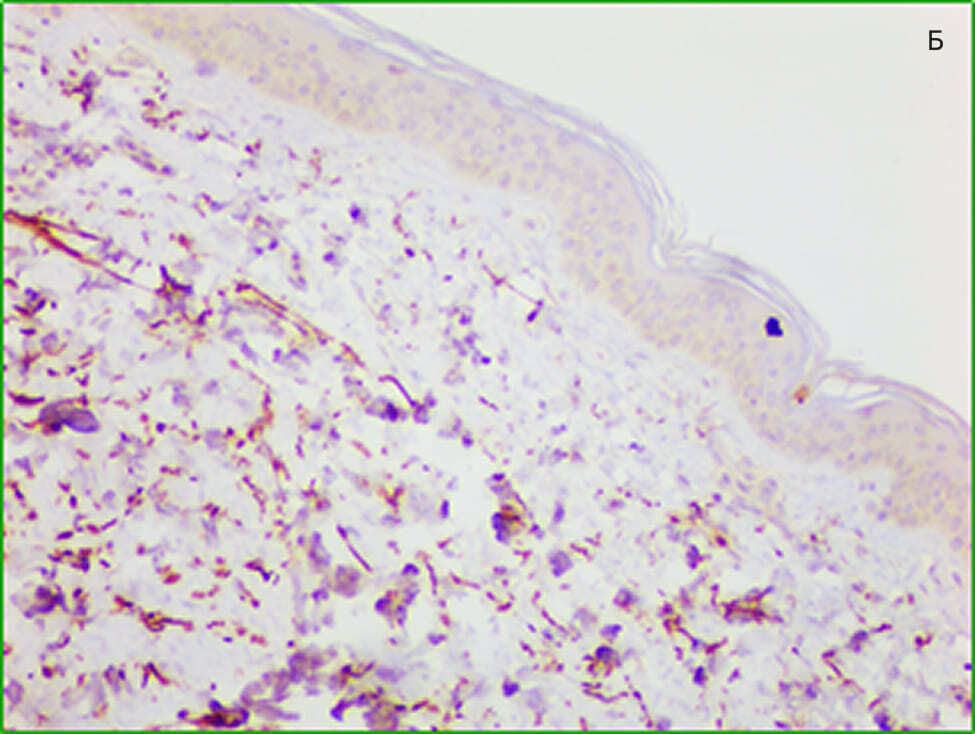
Рисунок 2. Результат иммунотипирования коллагена III. А — препарат до воздействия плазмой. слабо положительная реакция в мелких хаотично расположенных фокусах. Б — препарат после воздействия. Иммунореактивный продукт расположен вокруг капилляров и выводных протоков потовых желез. Стрептавидин-пероксидаза. Увеличение х 20.
Компьютерная морфометрия позволила установить, что объемная доля коллагена III типа в группе до лечения составила 4,7 [3,9; 5,6]%. В группе после лечения данный показатель достоверно увеличился до 8,4 [6,8; 9,9]%, что соответствует росту более чем в 1.8 раза (p=0.029). Результаты настоящего исследования демонстрируют выраженное положительное воздействие низкотемпературной аргоновой плазмы на процессы ремоделирования в гипертрофическом рубце, что согласуется с данными о биостимулирующих эффектах холодной плазмы в медицине [4, 5].
Исходная морфологическая картина соответствовала классическому описанию незрелого рубца с признаками хронического воспаления, что поддерживало дисбаланс синтеза и деградации ВКМ [1, 2]. Низкий базовый уровень коллагена III типа (4,7%) отражал относительную стабильность и низкую метаболическую активность патологического матрикса, характерную для сформированного рубца [3].
Проведенное исследование позволило выявить ключевые эффекты двукратного воздействия аргоновой плазмой:
Исходная морфологическая картина соответствовала классическому описанию незрелого рубца с признаками хронического воспаления, что поддерживало дисбаланс синтеза и деградации ВКМ [1, 2]. Низкий базовый уровень коллагена III типа (4,7%) отражал относительную стабильность и низкую метаболическую активность патологического матрикса, характерную для сформированного рубца [3].
Проведенное исследование позволило выявить ключевые эффекты двукратного воздействия аргоновой плазмой:
- Противовоспалительный эффект: Полное разрешение лимфомакрофагальной инфильтрации указывает на способность холодной плазмы прерывать хроническое воспаление — ключевое звено патогенеза рубцевания. Этот эффект, вероятно, опосредован модуляцией активности провоспалительных цитокинов и хемокинов под действием активных форм кислорода и азота (RONS), генерируемых плазмой [10].
- Активация ремоделирования ВКМ: Появление аморфного компонента и пучков зрелого коллагена свидетельствует о синхронной активации процессов деградации старого матрикса (возможно, за счет индукции матриксных металлопротеиназ) и синтеза нового [6]. Упорядочение волокон указывает на адекватное созревание коллагеновых волокон и нормализацию функции фибробластов.
- Стимуляция синтеза коллагена III типа: Наблюдаемое почти двукратное увеличение его доли является центральным находкой. Коллаген III типа — основной компонент ранней грануляционной ткани [3]. Его повышенная экспрессия интерпретируется как маркер перехода рубца в активную фазу репаративного ремоделирования, когда формируется новая, более физиологичная основа для последующего созревания. Данные литературы подтверждают, что физические воздействия, включая некоторые виды энергии, могут стимулировать синтез коллагена III типа фибробластами [11]. Полученные нами результаты количественно подтверждают эту способность применительно к холодной аргоновой плазме.
- Эпидермальный ответ: Развитие акантоза подтверждает биостимулирующее действие плазмы не только на дерму, но и на эпителий, что отмечалось и в других исследованиях [12].
06
Заключение
Таким образом, холодная аргоновая плазма выступает не как простой аблятивный агент, а как многофакторный стимулятор репаративной регенерации, сдвигающий патологический фиброз в сторону контролируемого заживления. Полученные данные подтверждают перспективность использования холодной аргоновой плазмы как метода, направленного на коррекцию не только клинических, но и гистологических проявлений патологического рубцевания, и служат основанием для дальнейших исследований с большей выборкой и изучением молекулярных механизмов.
07
Список литературы
G. G. Gauglitz et al., "Hypertrophic scarring and keloids: pathomechanisms and current and emerging treatment strategies," Mol Med, vol. 17, no. 1−2, pp. 113−125, 2011.
P. A. Khavkin and D. A. Ellis, "Aging skin: histology, physiology, and pathology," Facial Plast Surg Clin North Am, vol. 19, no. 2, pp. 229−234, 2011.
E. E. Tredget, B. Nedelec, P. G. Scott, and A. Ghahary, "Hypertrophic scars, keloids, and contractures. The cellular and molecular basis for therapy," Surg Clin North Am, vol. 77, no. 3, pp. 701−730, 1997.
G. Isbary et al., "A first prospective randomized controlled trial to decrease bacterial load using cold atmospheric argon plasma on chronic wounds in patients," Br J Dermatol, vol. 163, no. 1, pp. 78−82, 2010.
Bekeschus et al., "Medical gas plasma technology: Roadmap on cancer treatment and immunotherapy," Redox Biol, vol. 58, p. 102 508, 2022.
M. Keidar, "Plasma for cancer treatment," Plasma Sources Sci Technol, vol. 24, no. 3, p. 33 001, 2015.
J. D. Bancroft and M. Gamble, Theory and Practice of Histological Techniques, 7th ed. Churchill Livingstone, 2019.
S. Y. Tay and S. Y. Tan, "Immunohistochemistry techniques in the diagnosis and prognostication of melanoma," Indian J Dermatol, vol. 58, no. 5, p. 344, 2013.
Р. А. Чернышев, Е. А. Непомнящих, "Гистоморфологические аспекты репаративной регенерации кожи," Бюллетень сибирской медицины, т. 15, № 3, с. 129−140, 2016.
T. von Woedtke, S. Reuter, K. Masur, and K.-D. Weltmann, "Plasmas for medicine," Phys Rep, vol. 530, no. 4, pp. 291−320, 2013.
A. J. Singer and R. A. F. Clark, "Cutaneous wound healing," N Engl J Med, vol. 341, no. 10, pp. 738−746, 1999.
M. Heinlin et al., "Plasma medicine: possible applications in dermatology," J Dtsch Dermatol Ges, vol. 8, no. 12, pp. 968−976, 2010.
P. A. Khavkin and D. A. Ellis, "Aging skin: histology, physiology, and pathology," Facial Plast Surg Clin North Am, vol. 19, no. 2, pp. 229−234, 2011.
E. E. Tredget, B. Nedelec, P. G. Scott, and A. Ghahary, "Hypertrophic scars, keloids, and contractures. The cellular and molecular basis for therapy," Surg Clin North Am, vol. 77, no. 3, pp. 701−730, 1997.
G. Isbary et al., "A first prospective randomized controlled trial to decrease bacterial load using cold atmospheric argon plasma on chronic wounds in patients," Br J Dermatol, vol. 163, no. 1, pp. 78−82, 2010.
Bekeschus et al., "Medical gas plasma technology: Roadmap on cancer treatment and immunotherapy," Redox Biol, vol. 58, p. 102 508, 2022.
M. Keidar, "Plasma for cancer treatment," Plasma Sources Sci Technol, vol. 24, no. 3, p. 33 001, 2015.
J. D. Bancroft and M. Gamble, Theory and Practice of Histological Techniques, 7th ed. Churchill Livingstone, 2019.
S. Y. Tay and S. Y. Tan, "Immunohistochemistry techniques in the diagnosis and prognostication of melanoma," Indian J Dermatol, vol. 58, no. 5, p. 344, 2013.
Р. А. Чернышев, Е. А. Непомнящих, "Гистоморфологические аспекты репаративной регенерации кожи," Бюллетень сибирской медицины, т. 15, № 3, с. 129−140, 2016.
T. von Woedtke, S. Reuter, K. Masur, and K.-D. Weltmann, "Plasmas for medicine," Phys Rep, vol. 530, no. 4, pp. 291−320, 2013.
A. J. Singer and R. A. F. Clark, "Cutaneous wound healing," N Engl J Med, vol. 341, no. 10, pp. 738−746, 1999.
M. Heinlin et al., "Plasma medicine: possible applications in dermatology," J Dtsch Dermatol Ges, vol. 8, no. 12, pp. 968−976, 2010.
Читайте статьи:
30 Июня 2024
Новые технологии красоты


30 Июня 2024
Новые технологии красоты


30 Июня 2024
Новые технологии красоты


Все статьи из блога
Все статьи из блога









